药包材标准YBB的那些事
今天我们来谈下与药包材企业及药企比较关注的话题,也就是YBB的那些标准及存在的一些吐槽点,虽然说不敢“妄议国事”,但是,作为研发狗,法规狗来说,这些点,不得不提,也不得不面对。
YBB的框架结构


YBB,拼音里药(Y)包材(B)标准(B)三个首字母的简称,中间经历多次的变化,目前现行的为2015版,里面涵盖了玻璃类,金属类,塑料类,橡胶类,预灌封类,其它类与方法类七大部分。

图1 YBB 2015 药包材标准
对于每个部分,YBB的细分做得还是不错的,确实在编写时,也参考了一些不同的内容,往好的方面讲,是开放的,是整合各个标准的特点的。
目前YBB存在的一些槽点


参考标准,但是没有即时跟进标准
前面提到,YBB在制定时,大量参考了比如EP,USP,ISO等的内容,参考没有问题,但是如果没有跟进,就会无法与时俱进。其只有两个例子:
注射剂瓶中的垂直轴偏差
YBB00292005-2-2015:中硼硅玻璃管制注射剂瓶中,对于其中的垂直轴偏差,有如下的定义(图2),并且根据端肩与溜肩,进行了分类,两者的偏差有所不一。
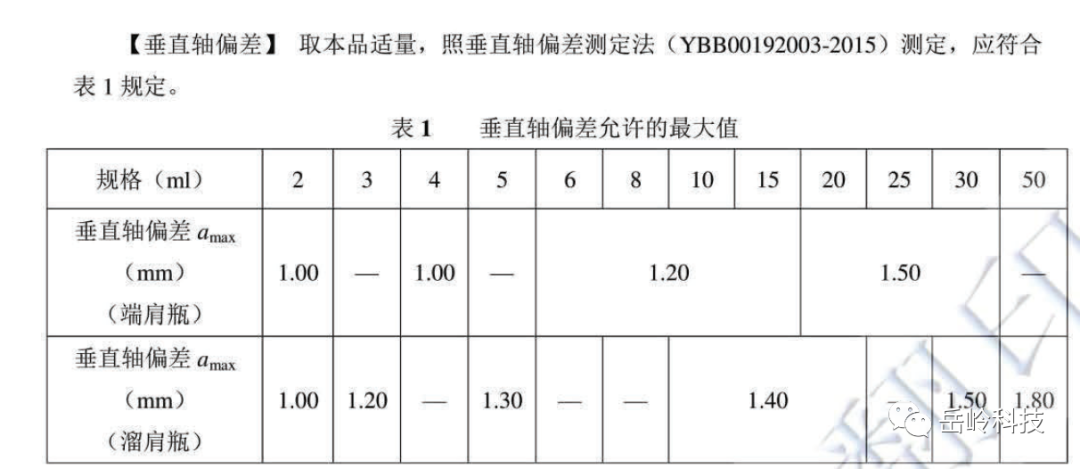
图2 YBB00292005-2-2015中的垂直轴偏差
再来看ISO8362-1,它中间出过多个版本,先看2009的版本,它就是YBB的原型,其垂直轴偏差(列名为a),YBB与它基本保持一致。
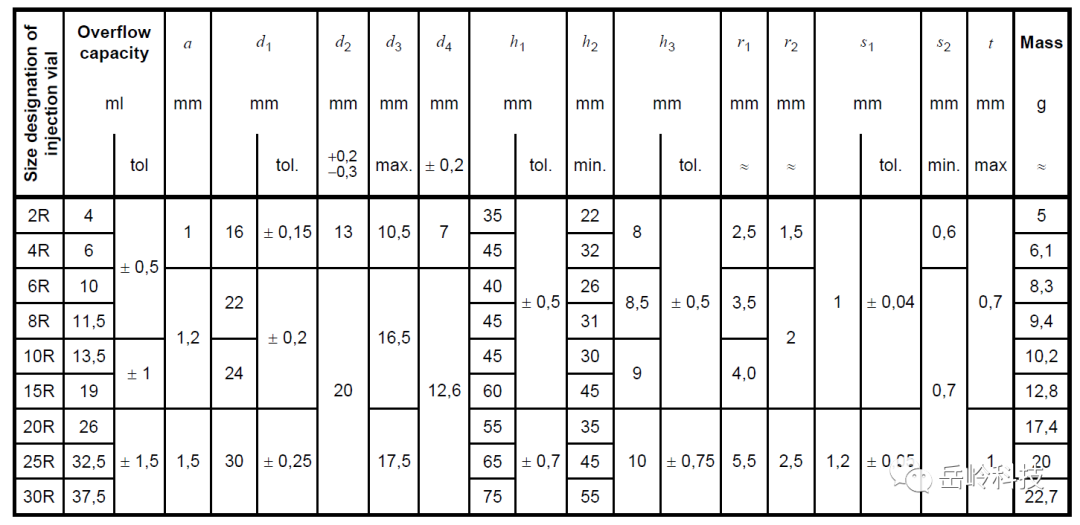
图3 ISO 8362-1 2009版的尺寸标准
再看后来的新ISO8362-1版本2018年,可以看到,里面的垂直轴偏差,已经更新了,新增加了3R,50R与100R。
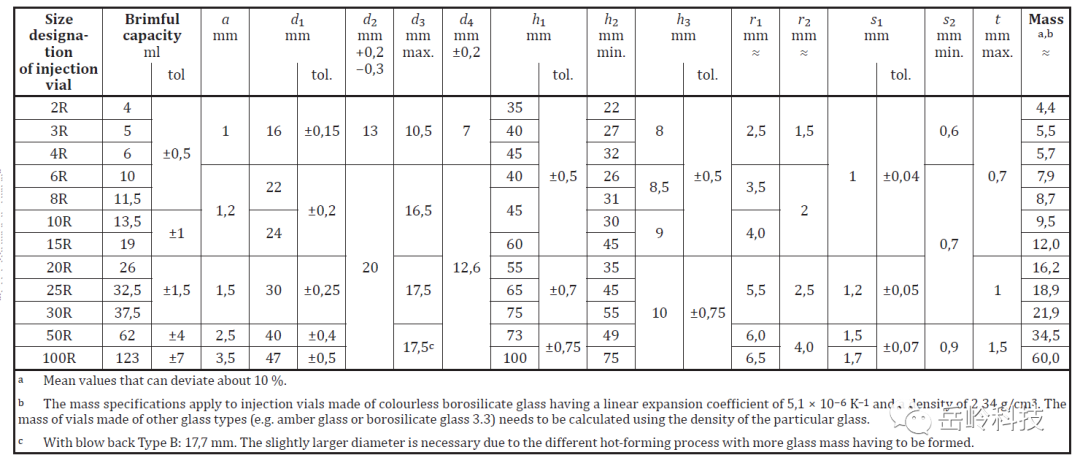
图4 ISO 8362-1 2018版的尺寸标准
所以,从法规标准的要求来看,如果有新的50R,100R,或者是3R,当国外已经在采用新的标准时,国内的YBB,还无法可依;另外,关于一些进口类的产品,国外COA上已经有新的标准,国内登记包材时,又是按照YBB,相当于要求变低了(因为没有要求);如果关于该要求,我们只是直接的加以引用,则不会存在这样的问题(随时跟随新版本),所以,这部分程度上阻碍了国际化的进步,反而不利于国内的发展。
参考标准,但不引用标准
这个不知道算不算槽点,但是,对于读者来说,如果想进一步跟进该方法的来源,就要自己反复去看,核对内容,这样就感觉不太舒适,至少从文献引用的方面来讲,是不够科学的。如果是ISO,或者其它的一些标准,多少会有一个章节Bibliography,方便读者去看原文,这样也是利于标准的不断进步的。

图5 标准中常有的引用文献
与国际接轨有待提高
因为YBB在制定时,加入了一些自己的“特色”,比如说低硼硅,中硼硅与高硼硅,在国际上都是统称Type 1玻璃,所以对于一些中美双报之类的问题,还得给国外的监管部门,解释什么叫中硼硅;关于其它的方面,比如说一些测试的细节,灭菌锅的升温降温速率等,也对一些要国内外同时申报的包材测试造成额外的工作负担。
以上观点仅是个人看法,如有不对可以留言指正。
未来可期


幸运的是,国家的监管部门,也意识到了这一点,也在向国际接轨方向在发展。
ChP2020就是一个开始,部分地纳入了一些包材的标准。国家药典委今年也启动了药包材标准的制定工作,按照凡例,通则和正文等三个层次加以编制;按照药包材通则,相关材料通则与通用测试方法的方式。
期待新的ChP2025能一统天下,然后有更好的国际接轨,解放药企与包材企业,让大家有更多的精力放在研发上。
参考文献:
1. T. Bauer,Encyclopedia of Modern Optics,2005, Pages 480-488
2.https://www.ondrugdelivery.com/polymer-syringe-considerations-for-drug-applications-and-administration/
3.http://www.jsyxmp.net/news/addnews3_5.html
4.https://www.xfdyb.com/list-14.html
5.https://www.plastics.gl/packaging/viable-for-vials/
